الاستوگرافی ؛ الاستوگرافی یا سونوگرافی الاستوگرافی برای بررسی سلامت بافت در کبد، پستان، تیروئید، کلیه، پروستات و غدد لنفاوی کاربرد دارد. تکنیکهای تصویربرداری مبتنی بر الاستوگرافی در سالهای اخیر برای ارزیابی غیرتهاجمی خواص مکانیکی بافت، مورد توجه قرار گرفتهاند. این تکنیک ها از تغییر خاصیت ارتجاعی بافت نرم در آسیب شناسی های مختلف برای به دست آوردن اطلاعات کمی و کیفی استفاده می کنند که می تواند برای اهداف تشخیصی استفاده شود. اندازهگیریها در حالتهای تصویربرداری تخصصی انجام میشوند که میتوانند سفتی بافت را در پاسخ به نیروی مکانیکی اعمال شده (فشرده یا موج برشی) تشخیص دهند.
برای رزرو نوبت جهت انجام الاستوگرافی در مرکز الوند با استفاده از بروزترین تجهیزات روز دنیا و کادری متخصص با ما تماس بگیرید.
روشهای مبتنی بر اولتراسوند(سونوگرافی) به دلیل مزایای ذاتی متعدد آن، مانند در دسترس بودن گسترده از جمله در کنار تخت و هزینه نسبتاً کم، از اهمیت ویژهای برخوردار هستند. چندین تکنیک الاستوگرافی اولتراسوند با استفاده از روش های مختلف تحریک توسعه داده شده است. به طور کلی، این ها را می توان به روش های تصویربرداری کرنشی که از محرک های فشرده سازی داخلی یا خارجی استفاده می کنند، و تصویربرداری موج برشی که از محرک های موج برشی سیار تولید شده توسط امواج فراصوت استفاده می کند، طبقه بندی کرد.
در حالی که الاستوگرافی اولتراسوند نتایج امیدوارکننده ای را برای ارزیابی غیرتهاجمی فیبروز کبدی نشان داده است، کاربردهای جدیدی در تصویربرداری پستان، تیروئید، پروستات، کلیه و غدد لنفاوی در حال ظهور است.
در اینجا، ما اصول اولیه، فیزیک پایه و محدودیتهای الاستوگرافی اولتراسوند را مرور میکنیم و کاربرد بالینی فعلی و پیشرفتهای جاری در کاربردهای مختلف بالینی را خلاصه میکنیم.
US:سونوگرافی معمولی
USE: سونوگرافی الاستوگرافی
مقدمه
الاستوگرافی اولتراسوند (USE) یک فناوری تصویربرداری حساس به سفتی بافت است که برای اولین بار در دهه 1990 توصیف شد. روشهای الاستوگرافی از تغییر الاستیسیته بافتهای نرم ناشی از فرآیندهای پاتولوژیک یا فیزیولوژیکی خاص بهره میبرند. برای مثال، بسیاری از تومورهای جامد از نظر مکانیکی با بافتهای سالم اطراف متفاوت هستند. به طور مشابه، فیبروز مرتبط با بیماری های مزمن کبدی باعث سفت شدن کبد نسبت به بافت های طبیعی می شود. از این رو می توان از روش های الاستوگرافی برای افتراق بافت آسیب دیده از طبیعی برای کاربردهای تشخیصی استفاده کرد.
سونوگرافی معمولی (US) این مزیت را دارد که یک روش ارزان، همه کاره و به طور گسترده در دسترس است که می تواند در کنار تخت استفاده شود، که در مورد USE نیز صدق می کند. USE برای چندین کاربرد بالینی در سالهای اخیر مورد بررسی قرار گرفته است و برای کاربردهای خاص مانند ارزیابی فیبروز کبدی یا مشخص کردن ضایعات پستان در روال بالینی معرفی شده است. تصویربرداری الاستیسیته توسط USE با افزودن سفتی به عنوان یکی دیگر از ویژگیهای قابل اندازهگیری به تکنیکهای تصویربرداری فعلی ایالات متحده، اطلاعات تکمیلی را برای ایالات متحده فراهم میکند.
در این بررسی، مروری بر اصول و مفاهیم USE ارائه میکنیم، تکنیکهای مختلف USE را توصیف میکنیم و کاربردهای بالینی USE را در کبد، پستان، تیروئید، کلیه، پروستات و غدد لنفاوی مورد بحث قرار میدهیم.
اصول و تکنیک های الاستوگرافی سونوگرافی
در ادامه خلاصهای از فیزیک USE و تکنیکهای فعلی ارائه میشود.
مقالات مرتبط:
تکنیک های الاستوگرافی سونوگرافی
از این اصول، تکنیکهای مختلف USE موجود در حال حاضر را میتوان با کمیت فیزیکی اندازهگیری شده طبقهبندی کرد (شکل 3):
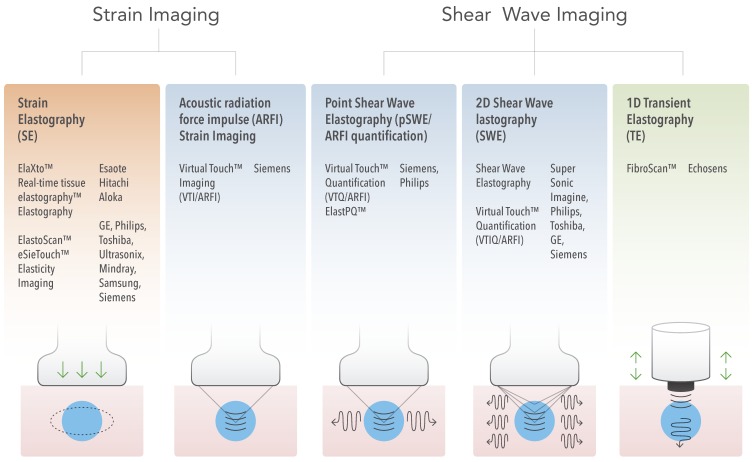
شکل 3-تکنیک های الاستوگرافی سونوگرافی. تکنیکهای USE موجود در حال حاضر را میتوان بر اساس کمیت فیزیکی اندازهگیری شده دستهبندی کرد: 1) تصویربرداری کرنش (چپ)، و 2) تصویربرداری موج برشی (راست). روشهای برانگیختگی شامل جابهجایی القای مکانیکی شبه استاتیک از طریق فشردهسازی فعال خارجی یا حرکت فیزیولوژیکی ناشی از غیرفعال (نارنجی)، فشردهسازی دینامیکی ناشی از مکانیکی از طریق یک مبدل کوبنده در سطح بافت برای تولید امواج برشی (سبز)، و اولتراسوند دینامیک است. القای جابجایی بافت و امواج برشی توسط تحریک تکانه نیروی تابش صوتی (آبی).
استرین الاستوگرافی
الاستوگرافی کرنشی را می توان با روش تحریک بیشتر تقسیم کرد:
1) در روش اول، اپراتور با مبدل اولتراسوند فشرده سازی دستی را روی بافت اعمال می کند. فشرده سازی دستی برای اندام های سطحی مانند سینه و تیروئید نسبتاً خوب عمل می کند، اما برای ارزیابی خاصیت ارتجاعی در اندام های واقع در عمق بیشتری مانند کبد چالش برانگیز است. .
2) در روش تحریک دوم، مبدل اولتراسوند ثابت نگه داشته می شود و جابجایی بافت توسط حرکت فیزیولوژیک داخلی (به عنوان مثال قلبی عروقی، تنفسی) ایجاد می شود. از آنجایی که این روش به فشرده سازی سطحی اعمال شده وابسته نیست، ممکن است برای ارزیابی اندام های عمیق تر استفاده شود.
سپس جابجایی بافت القایی در همان جهت تنش اعمال شده با تعدادی از روشهای مختلف وابسته به سازنده اندازهگیری میشود، از جمله ردیابی مبتنی بر همبستگی اکو فرکانس رادیویی (RF)، پردازش داپلر یا ترکیبی از این دو روش. ما ردیابی مبتنی بر همبستگی اکو RF را که یکی از رایجترین و سادهترین روشها است، مرور میکنیم. در این روش، خطوط دو بعدی RF A در امتداد محور جابجایی اندازه گیری می شوند. همبستگی سیگنال اکو RF بین پنجرههای جستجو در اکتسابهای مختلف امکان اندازهگیری جابجایی بافت Δl و تخمین کرنش نرمال εn را میدهد . پیشنهاد می شود مقاله سونوگرافی واژینال در تهران را مطالعه کنید
تصویربرداری کرنش ضربه نیروی تابش صوتی (ARFI).
این یک روش جایگزین برای اندازه گیری کرنش است. در این تکنیک از یک پالس فشاری (نیروی تابش صوتی) با مدت زمان کوتاه (0.1-0.5 میلیثانیه) با شدت بالا (میانگین پیک پالس فضایی = 1400 W/cm2، میانگین زمانی پیک مکانی = 0.7 W/cm2) استفاده میشود. جابجایی بافت (جابجایی ~ 10-20 میکرومتر) در جهت عادی، یعنی عمود بر سطح 12. جابجایی در یک ROI مشخص، متعاقباً با همان روشهایی که در الاستوگرافی کرنشی اندازهگیری میشود. همچنین، مشابه الاستوگرافی کرنشی، جابجایی ها ممکن است به صورت الاستوگرام روی تصویر 13 حالت B نمایش داده شوند. این رویکرد تصویربرداری برای مثال به عنوان تصویربرداری لمسی مجازی زیمنس (VTI) اجرا می شود.
تصویربرداری موج برشی
برخلاف تصویربرداری کرنش، که جابجایی بافت فیزیکی را به موازات تنش نرمال اعمال شده اندازهگیری میکند، SWI از یک تنش دینامیکی برای تولید امواج برشی در ابعاد موازی یا عمود استفاده میکند. اندازهگیری سرعت موج برشی به تخمینهای کمی و کیفی کشش بافت منجر میشود. در حال حاضر سه رویکرد فنی برای SWI وجود دارد: 1) الاستوگرافی گذرا یک بعدی (1D-TE)، 2) الاستوگرافی موج برشی نقطه ای (pSWE)، و 3) الاستوگرافی موج برشی دو بعدی (2D-SWE) . ویژگی های اصلی هر روش در شکل 4 خلاصه شده است. پیشنهاد میشود مقاله سونوگرافی سه بعدی رحم را مطالعه کنید
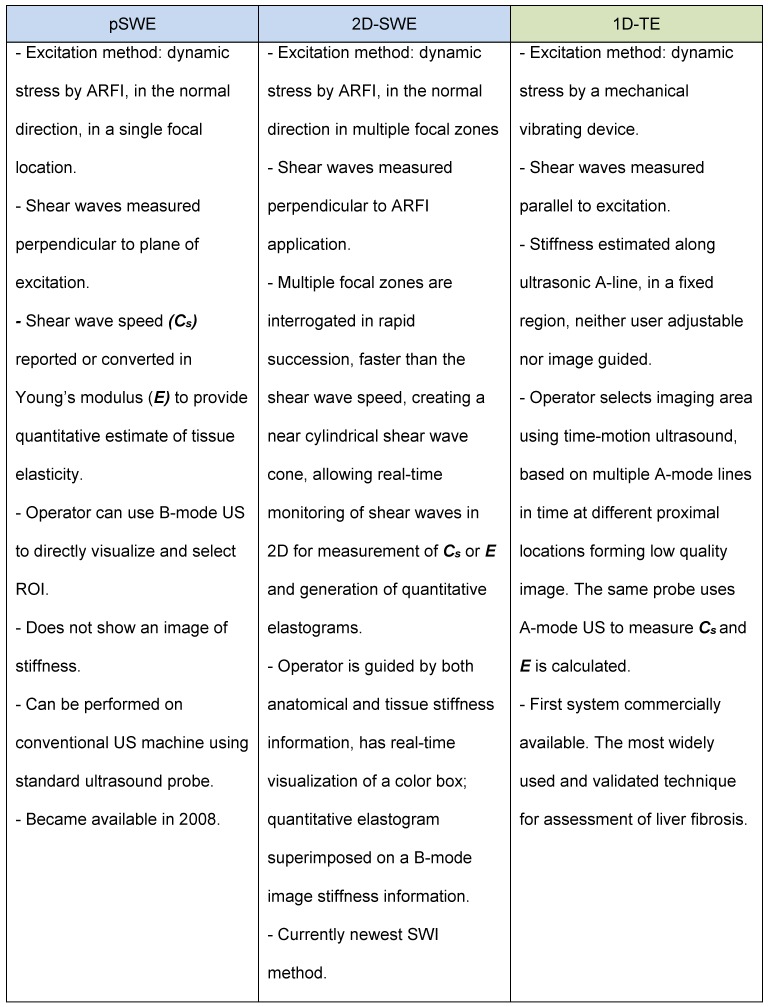
الاستوگرافی گذرا 1 بعدی
اولین سیستم SWI تجاری موجود، یک سیستم 1D-TE FibroScanTM (Echosens، پاریس، فرانسه) برای ارزیابی کبد 14 بود. این روش به طور گسترده مورد استفاده و تایید شده برای ارزیابی فیبروز کبد است، و اغلب توسط پزشکان در دفتر
پروب FibroscanTM یک دستگاه منفرد است که شامل یک مبدل اولتراسوند و یک دستگاه لرزاننده مکانیکی است. اگرچه 1D-TE یک تکنیک مبتنی بر ایالات متحده است، اما بدون هدایت تصویر مستقیم حالت B استفاده می شود. اپراتور ناحیه تصویربرداری را با استفاده از اولتراسوند حرکت زمانی (بر اساس خطوط چندگانه A-mode در زمان در مکانهای مختلف نزدیک که برای تشکیل تصویری با کیفیت پایین جمع شدهاند) انتخاب میکند تا قسمتی از کبد را در 2.5 تا 6.5 سانتیمتر زیر سطح پوست و عاری از موارد بزرگ قرار دهد. ساختارهای عروقی سپس دستگاه ارتعاشی مکانیکی یک "پانچ" خارجی ارتعاشی کنترل شده روی سطح بدن اعمال می کند تا امواج برشی ایجاد کند که در بافت منتشر می شود. سپس همان کاوشگر از حالت A برای اندازهگیری سرعت موج برشی استفاده میکند و مدول یانگ E 15 محاسبه میشود. اندازهگیریها حجم بافت تقریباً 1 سانتیمتر عرض x 4 سانتیمتر طول را ارزیابی میکنند که بیش از 100 برابر بزرگتر از حجم متوسط است. نمونه بیوپسی 16، 17. معاینهکننده اندازهگیریهای مکرر را با معیارهای زیر برای اعتبارسنجی انجام میدهد: (1) حداقل 10 اندازهگیری معتبر، (2) نسبت تعداد اندازهگیریهای معتبر به تعداد کل اندازهگیریها ≥ 60% است (3) محدوده بین چارکی (IQR)، که منعکس کننده تغییرپذیری اندازه گیری ها است، کمتر از 30 درصد از مقدار متوسط اندازه گیری های سفتی کبد است 16. کل معاینه تقریباً 5 دقیقه طول می کشد.
الاستوگرافی موج برشی نقطه ای
در این تکنیک، از ARFI برای القای جابجایی بافت در جهت طبیعی در یک مکان کانونی، مشابه تصویربرداری کرنش ARFI استفاده میشود. برخلاف تصویربرداری کرنش ARFI، خود جابجایی بافت اندازهگیری نمیشود. در عوض، بخشی از امواج طولی تولید شده توسط ARFI از طریق جذب انرژی صوتی به امواج برشی تبدیل می شود. مدول E و برآورد کمی از کشش بافت گزارش شده است.
برخلاف 1D-TE، pSWE را می توان بر روی یک دستگاه سونوگرافی معمولی با استفاده از پروب سونوگرافی استاندارد 17 انجام داد.
در کاربردهای کبدی، مزایای متعددی از pSWE در مقایسه با 1D-TE وجود دارد. اول، اپراتور میتواند از B-mode US برای تجسم مستقیم کبد برای انتخاب ناحیه یکنواخت پارانشیم کبد بدون عروق بزرگ یا مجاری صفراوی گشاد شده استفاده کند. همچنین، بر خلاف 1D-TE که امواج برشی با تحریک در سطح بدن تولید میشوند، pSWE امواج برشی را تولید میکند که به صورت موضعی در داخل کبد منشا میگیرند و باعث میشود pSWE کمتر تحت تأثیر آسیت و چاقی 5، 6، 18 قرار گیرد.
در حال حاضر، دو محصول تجاری با استفاده از pSWE وجود دارد: Virtual TouchTM Quantification (VTQ/ARFI) توسط زیمنس که از سال 2008 در دسترس است و Elast-PQTM جدیدتر توسط Philips که در سال 2013 معرفی شد.
مطالب پیشنهادی :
الاستوگرافی موج برشی دو بعدی (2 بعدی).
SWE دو بعدی (2D) جدیدترین روش SWI در حال حاضر است که از نیروی تابش صوتی استفاده می کند. به جای یک مکان کانونی واحد مانند تصویربرداری کرنش ARFI و pSWE، چندین ناحیه کانونی بهسرعت، سریعتر از سرعت موج برشی مورد بررسی قرار میگیرند. این یک مخروط موج برشی تقریباً استوانهای ایجاد میکند که امکان نظارت در زمان واقعی امواج برشی را به صورت دو بعدی برای اندازهگیری سرعت موج برشی یا مدول E یانگ و تولید الاستوگرامهای کمی 4 فراهم میکند. تا به امروز، سیستمهای تجاری موجود زیر از فناوری 2D-SWE استفاده میکنند: Virtual TouchTM Imaging Quantification (VTIQ/ARFI) توسط زیمنس، Shear WaveTM Elastography توسط SuperSonic Imagine (SSI)، Elastography موج برشی توسط Philips، Acoustic Structure QuantificationTM (ASQ) توسط Toshiba، و 2D-SWE توسط GE Healthcare 2، 4.
مزایای این تکنیک شامل تجسم بلادرنگ یک الاستوگرام کمی رنگی است که بر روی تصویر B-mode 19 قرار گرفته است، که اپراتور را قادر میسازد با اطلاعات آناتومیکی و سفتی بافت 20 هدایت شود.
محدودیت های فنی الاستوگرافی سونوگرافی
با افزایش علاقه بالینی به توسعه کاربردهای USE جدید، یا اصلاح برنامههای موجود، درک محدودیتهای فنی فعلی که مانع تکرارپذیری اندازهگیری میشوند، ضروری است. چندین عامل مخدوش کننده فنی بر روی USE تأثیر می گذارند. تعدادی از این موارد را می توان به محدودیت های کلی سونوگرافی مانند سایه، طنین، و مصنوعات درهم و برهم، یا ماهیت وابسته به اپراتور سیستم های اولتراسوند دست آزاد ردیابی کرد. به طور مشابه، تضعیف بافت سیگنال اولتراسوند را به عنوان تابعی از عمق کاهش می دهد.
محدود کردن ارزیابی دقیق بافت یا اندام های عمیق تر. چربی مایع یا زیر جلدی همچنین انتشار محرک خارجی اعمال شده در سطح پوست (به عنوان مثال FibroscanTM) را کاهش می دهد، که می تواند اندازه گیری ها را در شرایط چاقی یا آسیت شکمی باطل کند. .) همچنین می تواند نتایج مغرضانه ای را در صورت عدم استانداردسازی در گروه های بیمار و نقاط زمانی در کاربردهای طولی ایجاد کند. علاوه بر این، فقدان یکنواختی طراحی و تنظیمات سیستم تجاری، مقایسه اندازهگیریها از یک سیستم سازنده به سیستم دیگر را به یک کار دشوار تبدیل میکند . برای مثال، ابتکاری توسط اتحاد نشانگرهای زیستی تصویربرداری کمی (QIBA) در تلاش است تا از فانتومها برای استانداردسازی اندازهگیریهای کمی از تکنیکهای مختلف USE استفاده کند .
از روشهای USE که در بالا توضیح داده شد، اندازهگیریهای روشهایی که از محرکهای خارجی استفاده میکنند، مانند الاستوگرافی فشاری، چالش برانگیزترین برای بازتولید هستند. اندازهگیریها در این حالتها بسیار ذهنی هستند، زیرا کنترل بزرگی تنش اعمالشده با فشردهسازی دستی وابسته به اپراتور و تغییرپذیری ذاتی حرکت فیزیولوژیک زمانی که به عنوان محرک استفاده میشود، دشوار است. انتخاب ROI نیز وابسته به اپراتور است و میتواند تغییرپذیری را ایجاد کند 18. بعلاوه، میزان تنش ناشی از یک اپراتور میتواند منجر به ایجاد آرتیفکتهای غلظت کرنش در اطراف ساختارهای خاص شود، که سپس میدان کرنش را مخدوش کرده و مصنوعاتی را در تصاویر یا اندازهگیریهای اشتباه ایجاد میکند.
در نتیجه، روشهای SE فقط به ارزیابیهای نیمه کمی سختی اجازه میدهند که مقایسه طولی آن دشوار است. الاستوگرافی به طور کلی به منابع داخلی استرس (به عنوان مثال قلبی، تنفس) نیز حساس است. به عنوان مثال در کاربردهای کبدی، اندازه گیری سفتی در لوب راست نسبت به لوب چپ برای به حداقل رساندن تحریکات داخلی ایجاد شده توسط قلب نزدیک که می تواند منجر به اندازه گیری اشتباه شود، ترجیح داده می شود. در مورد حالتهای الاستوگرافی که از منابع داخلی استرس تحریک (به عنوان مثال قلبی) استفاده میکنند که توسط اپراتور قابل تنظیم نیست، مهم است که توجه داشته باشیم که این تنشها پیچیده، کمی کردن آن دشوار است و در طول زمان متغیر هستند (به عنوان تابعی از فیزیولوژی). ، بنابراین می تواند پاسخ های کرنش اندازه گیری شده را دستکاری کند.
علاوه بر این، حالتهای USE موجود تجاری بر مجموعهای از مفروضات در مورد مواد بافتی که مورد بررسی قرار میگیرند تکیه میکنند تا تجزیه و تحلیل و تفسیر اندازهگیریها/تصویربرداری را سادهتر کنند. مفروضات اصلی این است که بافت عبارت است از:
- خطی؛ کرنش حاصل به صورت خطی به عنوان تابعی از تنش افزایشی افزایش می یابد (معادله 1)
- کشسان؛ تغییر شکل بافت وابسته به نرخ تنش نیست و بافت به حالت تعادلی بدون تغییر شکل اولیه باز می گردد.
- ایزوتروپیک؛ بافت متقارن/همگن است و به تنش از همه جهات یکسان پاسخ می دهد
- تراکم ناپذیر؛ حجم کلی بافت تحت فشار اعمال شده یکسان باقی می ماند.
تا به امروز، این مفروضات در سناریوهای بالینی خاص (به عنوان مثال فیبروز) وجود داشته است، اما نشان داده شده است که در سایر کاربردهای تصویربرداری (مثلاً در بیماران با شاخص توده بدنی بالا) شکست خورده است. خواص مکانیکی بافت نرم بهعنوان مواد پیچیده و ناهمگنی که در هنگام کاوش، واکنش مکانیکی چسبناک و الاستیک دارند. سفتی بافت با فشردگی افزایش مییابد، که منجر به کاهش کرنش و افزایش سرعت موج برشی 2، 4 میشود. این فرض که بافت همسانگرد (همگن) است در رابطهای بافتی نقض میشود، جایی که انعکاس موج برشی در رابطهای ساختاری ممکن است منجر به تخمینهای نادرست سرعت شود.
تراکم نادرست است زیرا بافت ها هنگام فشرده شدن می توانند حجم خود را از دست بدهند (معمولاً به شکل مایع). در نهایت، فرض الاستیسیته بافت خالص، حضور ویسکوزیته بافت را نادیده میگیرد، که وابستگی سرعت موج برشی به فرکانس تحریک را معرفی میکند. این وابستگی مقایسه اندازهگیریهای سرعت موج برشی را در میان فروشندگان مختلف ایالات متحده که از فرکانسهای تحریک متفاوت استفاده میکنند، پیچیده میکند. همچنین، اگرچه پیشفرضهای انجامشده تا به امروز فرآیند تصویربرداری/اندازهگیری الاستوگرافی را تسهیل میکنند، احتمالاً این تصاویر نادرست از مکانیک بافت هستند. پذیرش الاستوگرافی برای کاربردهای بالینی جدید، مانند مشخص کردن تودهها یا اندامهای تومور بسیار ناهمگن، احتمالاً نیازمند اتخاذ مدلسازی پیچیدهتر است که ویسکوالاستیسیته بافت را به حساب میآورد . شامل نواحی الاستیک سفت (مانند فیبروز، کلسیفیکاسیون) و همچنین نواحی چسبناک نرم (مانند حوضچه های خون، نواحی دژنراسیون کیستیک) با تغییرات در مقیاس های طولی مختلف است.
با این وجود، USE یک روش امیدوارکننده است که در حال توسعه سریع و تحقیقات فعال است. علیرغم محدودیتهایی که در بالا توضیح داده شد، USE نوید بالینی بسیار خوبی دارد زیرا اندازهگیریها همبستگی قابلتوجهی با وضعیتهای بیماری منتشر و کانونی در اندامهای متعدد نشان دادهاند.
با درک اصول و تکنیکهای فیزیکی اولیه USE، در مرحله بعد عملکرد USE را در کبد، پستان، تیروئید، کلیه، پروستات و غدد لنفاوی بررسی میکنیم.
مقالات پیشنهادی :
کاربردهای بالینی الاستوگرافی سونوگرافی کبد
بیماری مزمن کبد (CLD) یک مشکل عمده بهداشت عمومی در سراسر جهان است. در ایالات متحده، CLD دوازدهمین علت مرگ و میر در سال 2013 بود که 1.4 درصد از کل مرگ و میرها را به خود اختصاص داد. یک مسیر مشترک به سمت فیبروز کبدی و در نهایت سیروز، افزایش خطر ابتلا به فشار خون پورتال (PH)، نارسایی کبدی، و کارسینوم سلولی کبدی (HCC) . با این وجود، فیبروز کبدی را می توان معکوس کرد، تثبیت کرد، یا در صورت ایجاد علت زمینه ای از آن جلوگیری کرد. فیبروز کبدی برداشته می شود و/یا بیمار با داروهای سرکوب کننده سیستم ایمنی، ضد التهابی یا ضد ویروسی یا با عوامل ضد فیبروتیک کمکی جدید مانند آنتی اکسیدان ها و مهارکننده های آنژیوتانسین درمان می شود.
در حال حاضر، بیوپسی کبد بهترین استاندارد مرجع موجود برای ارزیابی و طبقه بندی مراحل فیبروز/سیروز کبدی است، با امتیاز METAVIR که به طور گسترده مورد استفاده قرار می گیرد سیستم درجه بندی هیستوپاتولوژیک است. طبق این سیستم مراحل فیبروز عبارتند از: F0= کبد طبیعی، F1= فیبروز حداقل، F2= فیبروز قابل توجه، F3= فیبروز شدید و F4= سیروز. با این حال، بیوپسی کبد دارای چندین محدودیت است. تهاجمی است و در حدود 20 درصد موارد می تواند عوارض جزئی از جمله درد موقت ایجاد کند. عوارض عمدهای مانند خونریزی، هموبیلی، پریتونیت صفراوی، باکتریمی، سپسیس، پنوموتوراکس، هموتوراکس و حتی مرگ در 1.1 درصد از نمونهبرداریهای کبد رخ میدهد. 1/50000 از کل حجم کبد 19، 34. توافق بین ناظران بین پاتولوژیست ها در درجه بندی فیبروز/سیروز کبدی نیز کامل نیست، با آمار کاپا از 0.5 تا 0.9 بسته به تخصص پاتولوژیست 35.
مرحله بندی دقیق فیبروز/سیروز کبدی مهم است زیرا توصیه های درمانی بسته به نوع CLD متفاوت است. شواهد از درمان برای همه بیماران آلوده به ویروس هپاتیت C (HCV) پشتیبانی می کند. با این حال، در مکان هایی که منابع محدود است، از مرحله فیبروز کبدی برای اولویت بندی درمان استفاده می شود. به عنوان مثال، بیماران مبتلا به فیبروز F3 یا F4 به دلیل خطر عوارض شدید در بالاترین اولویت برای درمان قرار دارند، در حالی که بیماران مبتلا به فیبروز F2 به دلیل خطر نسبتاً کمتر عوارض، در اولویت درمان قرار دارند. (HBV)، بیماران با حداقل فیبروز F2 و HBV DNA > 2000 IU/ml برای درمان ضد ویروسی در نظر گرفته می شوند، حتی اگر سطح آلانین آمینوترانسفراز (ALT) آنها کمتر از دو برابر حد بالای نرمال 37 باشد. یک آزمایش کمی غیر تهاجمی مانند USE که امکان نظارت طولی دقیق سفتی کبد را فراهم می کند، از نظر بالینی با این تصمیمات درمانی مفید خواهد بود.
از آنجایی که با پیشرفت فیبروز به دلیل رسوب کلاژن و تغییرات ریزساختاری، کبد سفتتر میشود، USE این پتانسیل را دارد که این تغییرات هیستوپاتولوژیک را از طریق اندازهگیریهای کمی غیرتهاجمی سختی کبد، با استفاده از مقادیر مختلف برش سختی برای شبیهسازی امتیاز METAVIR، پایش کند. با این حال، USE دارای محدودیت هایی برای تمایز بین مراحل متوالی است که در ادامه بیشتر توضیح داده خواهد شد.
ارزیابی فیبروز کبد با تکنیک های مختلف الاستوگرافی کبد
یک روش استاندارد الاستوگرافی کبد برای به دست آوردن نتایج قابل اعتماد و دقیق بسیار مهم است. از بیمار در وضعیت خوابیده به پشت یا خفیف (30 درجه) سمت چپ، با بازوی راست بالای سر برای باز کردن فضاهای بین دنده ای و بهبود پنجره صوتی به کبد تصویربرداری می شود. از آنجایی که حرکت قلب میتواند اندازهگیریهای الاستوگرافی را مخدوش کند، توصیه میشود از اندازهگیریها در لوب راست کبد نمونه برداری شود، که مطمئنترین نتایج را نشان داده است. هنگام استفاده از تکنیکهای SWE، پالس فشار نیروی تشعشع صوتی باید عمود بر کپسول کبد اعمال شود، با اندازهگیریهایی که در عمق 4-5 سانتیمتری پوست و حداقل 1-2 سانتیمتر از پارانشیم کبد به دست میآید تا انکسار نبض محدود شود. از آنجایی که بافت ارزیابی شده 1.0 سانتی متر بالا و پایین ROI تعیین شده توسط کاربر گسترش می یابد، اپراتور باید بررسی کند که این نواحی فاقد ساختارهای عروقی و صفراوی و سایه های دنده هستند. علاوه بر این، بیمار باید در تنفس آموزش داده شود (برای توقف تنفس در پایان بازدم یا دم طبیعی) بنابراین اندازهگیریها در موقعیت خنثی انجام میشوند، زیرا مانور والسالوا یا بازدم عمیق میتواند بهطور کاذب اندازهگیری سفتی را افزایش دهد.
الاستوگرافی گذرا 1 بعدی کبد
مطالعات TE یک بعدی نشان داده است که مقادیر سفتی کبد با مراحل فیبروز هیستوپاتولوژیک در بیماران CLD همبستگی دارد (جدول (جدول 1).1). یک مطالعه 2 فازی چند مرکزی اخیر در ایالات متحده در بیماران مبتلا به HCV (n = 700) یا HBV (n = 53) 1D-TE را با بیوپسی کبد مقایسه کرد. در فاز 1 مطالعه، مقادیر برش سختی بهینه برای شناسایی فیبروز F2 تا F4 شناسایی شد، و در فاز 2 مقادیر برش در گروه دوم و بیماران مختلف مورد آزمایش قرار گرفت (جدول (جدول 11،40). 1D. -TE در گروه HCV (AUROC F≥2 0.89، F≥3 0.92، F4 0.92) و در گروه HBV (F≥2 0.73، F≥3 0.83، F≥2، 0.73، F≥3، 0.83، منطقه نسبتاً بالایی زیر منحنیهای مشخصه عملکرد گیرنده (AUROCs) سطح نسبتا بالایی را نشان داد. F4 0.90)، نتایج قبلی را تأیید می کند که نشان می دهد 1D-TE امکان مرحله بندی فیبروز قابل توجه را فراهم می کند. ≥3 0.89, F4 0.93) . متاآنالیز دیگری از 50 مطالعه در بیماران با علل مختلف CLD (n=518) با استفاده از بیوپسی کبد به عنوان استاندارد مرجع، نشان داد که 1D-TE دقیقتر است. در تشخیص فیبروز F4 نسبت به فیبروز F2 یا F3 (AUROC F4 0.93 در مقابل F≥2 0.87، F≥3 0.91)، صرف نظر از علت زمینه ای دی کبد دریا . به طور کلی، 1D-TE برای تشخیص سیروز (فیبروز F4) و برای تشخیص فیبروز قابل توجه (≥ F2) از غیر قابل توجه (F0 و F1) مفید است. با این حال، تمایز بین مراحل فیبروز فردی هنوز به خوبی تایید نشده است.
مقالات پیشنهادی :
الاستوگرافی موج برشی نقطه ای کبد
مطالعات منتشر شده pSWE به طور کلی نتایج خوبی را در ارزیابی فیبروز کبد نشان داده است، با اکثر مطالعات از VTQ/ARFI (جدول (جدول 1).1). متاآنالیز مطالعات pSWE (VTQ/ARFI) شامل 518 بیمار مبتلا به CLD اثبات شده با بیوپسی عمدتاً از HCV، AUROCهای F≥2 0.87، F≥3 0.91 و F=4 0.93 را نشان داد (جدول (جدول 11،17). همان متاآنالیز زیرمجموعه ای از 312 بیمار را که با هر دو pSWE (VTQ/ARFI) و 1D-TE (FibroScanTM) ارزیابی شدند، مقایسه کرد و دریافت که 1D-TE در تشخیص فیبروز قابل توجه کمی دقیق تر از pSWE است (AUROC 0.92 در مقابل 0.87) و سیروز (0.97 در مقابل 0.93) (جدول (جدول 11،17). در مقابل، متاآنالیز دیگری که شامل 1163 بیمار مبتلا به CLD بود نشان داد که pSWE (VTQ/ARFI) ارزش پیش بینی مشابهی را با 1D- نشان داد. TE برای فیبروز قابل توجه (AUROC 0.74 در مقابل 0.78) و سیروز (0.87 در مقابل 0.89) (جدول 1،44).
الاستوگرافی موج برشی دو بعدی کبد
در میان چهار سیستم ایالات متحده که دارای 2D-SWE هستند (همانطور که در بالا توضیح داده شد)، الاستوگرافی Shear WaveTM توسط SuperSonic Imagine (SSI) در حال حاضر معتبرترین سیستم برای ارزیابی فیبروز کبد است. اولین مطالعه با مقایسه 2D-SWE (SSI) و 1D-TE در 121 بیمار مبتلا به HCV مزمن با استفاده از بیوپسی کبد به عنوان استاندارد مرجع انجام شد. 2D-SWE در ارزیابی فیبروز قابل توجه (F≥2) دقیق تر از 1D-TE بود (AUROC 0.92 در مقابل 0.84؛ p=0.002) 20، با مقادیر برش بهینه برای 2D-SWE که در جدول 2 خلاصه شده است. 2. در یک مطالعه مقایسه آینده نگر درون فردی با مقایسه 2D-SWE (SSI)، pSWE (VTQ/ARFI) و 1D-TE (FibroscanTM) در 349 بیمار متوالی و با استفاده از نمونه برداری از کبد به عنوان استاندارد طلا، 2D-SWE دارای تشخیص بالاتری بود. دقت از 1D-TE در تشخیص فیبروز شدید (F≥3) (AUROC 0.93 در مقابل 0.87؛ p=0.0016، به ترتیب) و بالاتر از pSWE در تشخیص فیبروز قابل توجه (F≥2) (AUROCs 0.88 در مقابل 0.81؛ p = 0.0003). مقادیر برش بهینه مورد استفاده در این مطالعه در جدول 11 45 خلاصه شده است. در مطالعه دیگری (جدول 1،1، 46) تفاوت معنی داری در AUROCs برای 2D-SWE، pSWE و 1D-TE در تشخیص فیبروز قابل توجه (F≥2: 0.87، 0.92، 0.91)، فیبروز پیشرفته (F≥3: 0.91، 0.93، 0.94) و سیروز کبدی (F=4: 0.88، 0.90، 0.89 0.89) بین سه روش .
مقایسه نتایج بهدستآمده با تکنیکهای مختلف الاستوگرافی چالشبرانگیز است زیرا اصطلاحات، پارامترهای گزارششده، فرکانس موج برشی و سایر عوامل فنی استاندارد نشدهاند. برای مثال، برخی از تکنیکهای مبتنی بر SWE واحدهای متفاوتی را گزارش میکنند (مانند m/s یا kPa) 6 و مقادیر برش متفاوتی را اعمال کنید که توسط هر سازنده تعریف شده است و می تواند بین سیستم ها متفاوت باشد همانطور که در جدول 2.2 خلاصه شده است. کمیته فنی سرعت موج برشی فراصوت انجمن رادیولوژی آمریکای شمالی در تلاشی برای کمیت کردن تفاوتهای بین سیستمهای دارای سرعت موج برشی بالینی تجاری (SWS) (FibroscanTM، Philips، Siemens S2000، SSI Aixplorer) و همچنین سیستمهای آزمایشی اتحاد نشانگر زیستی تصویربرداری کمی (QIBA) از آزمایشهای مکانیکی دینامیکی مواد فانتوم استفاده کرد. سرعت موج برشی به صورت جفت فانتوم (یک فانتوم نرم و یک فانتوم سخت) در سه عمق تخمین زده شد. تفاوت آماری معنی داری در تخمین SWS در بین سیستم ها و با عمق فانتوم وجود داشت (در همه سیستم های تصویربرداری نشان داده شده است). نتایج نشان میدهد که تفاوت در اندازهگیریها بین ماشینها و ناظران میتواند در حدود ۱۲٪ متفاوت باشد. این یافته ها هنوز در مطالعات بالینی تایید نشده اند.
مقالات پیشنهادی :
کمی سازی فشار خون پورتال
فشار خون پورتال (PH) یکی از مهمترین عوارض CLD و سیروز است. هنگامی که فشار پورتال و گرادیان فشار ورید کبدی (HVPG) به سطحی افزایش مییابد که بدن نمیتواند آن را جبران کند، عوارضی مانند آسیت، خونریزی واریس و آنسفالوپاتی کبدی ممکن است ایجاد شود. در معرض خطر بالای ابتلا به واریس. در HVPG ≥ 12 میلیمتر جیوه، PH شدید با افزایش خطر خونریزی حاد واریسی تعریف میشود که میزان مرگ و میر آن تقریباً 15٪ است. تکنیک ها و همچنین آندوسکوپی دستگاه گوارش فوقانی برای ارزیابی وجود و درجه واریس مری 49. هر دو تست تهاجمی هستند.
الاستوگرافی اولتراسوند ممکن است با اندازه گیری سفتی کبد (LS) و/یا سفتی طحال (SS) به یک جایگزین غیر تهاجمی تبدیل شود. در SS، همان تکنیک هایی که در بالا برای کبد توضیح داده شد در طحال اعمال می شود. مطالعات اخیر با استفاده از 1D-TE نشان داد که LS برای تشخیص PH قابل توجه بالینی دقیق تر از SS است (AUROCs 0.95 در مقابل 0.85 50؛ 0.78 در مقابل 0.63 51). در مقابل، مطالعه دیگری بر روی 60 بیمار سیروزی که با pSWE مورد بررسی قرار گرفتند و از HVPG به عنوان استاندارد مرجع استفاده کردند، نشان داد که SS دقیقترین تست در تشخیص بالینی مهم (AUROC: 0.943) و PH شدید (AUROC: 0.963) است. 47. در آن مطالعه مقادیر برش SS m/s 3.36 و m/s 3.51 بیماران مبتلا به واریس مری و واریس مری پرخطر را به ترتیب با ارزش اخباری منفی 96.6% و 97.4% شناسایی کردند. چندین مطالعه اضافی نشان داده اند که SS پیش بینی کننده واریس مری است. به عنوان مثال، مطالعه ای با استفاده از pSWE طحال در 340 بیمار سیروزی و 16 داوطلب سالم با آندوسکوپی تهاجمی به عنوان استاندارد مرجع نشان داد که یک مقدار برش سرعت موج برشی 3.30 متر بر ثانیه، واریس مری پرخطر را با ارزش اخباری منفی شناسایی کرد. ، حساسیت و دقت به ترتیب 0.994، 0.989 و 0.721 52. نتایج کلی نشان می دهد که هر دو SS و LS پارامترهای امیدوارکننده ای هستند که ممکن است امکان غربالگری غیرتهاجمی برای PH و وجود واریس مری را فراهم کنند. برای تأیید بیشتر نتایج فعلی و ارزیابی اینکه آیا LS، SS، یا ترکیبی از این دو منجر به دقیقترین ارزیابی میشود، به مطالعات بیشتری نیاز است.
مشخصات ضایعات کانونی کبد
در حال حاضر، استفاده از الاستوگرافی اولتراسوند برای شناسایی ضایعات کانونی کبد (FLLs) هنوز در حال بررسی است، اما چند مطالعه نتایج امیدوارکنندهای را نشان دادهاند (جدول (جدول 33).
متاآنالیز 6 مطالعه (4 مطالعه با استفاده از pSWE، 2 SE) با بافت شناسی به عنوان استاندارد طلایی نشان داد که حساسیت، ویژگی، نسبت احتمال مثبت (LR) و LR منفی الاستوگرافی برای تمایز ضایعات بدخیم از خوش خیم ترکیب شده است. 85٪، 84٪، 5.69 و 0.17، به ترتیب، با AUROC خلاصه 0.93 (جدول (جدول 3،3، 53). در مطالعه اخیر دیگری، مقدار برش 2.52 متر بر ثانیه با استفاده از VTQ/ARFI اجازه تمایز را می دهد. FLL های بدخیم از خوش خیم با حساسیت و ویژگی به ترتیب 97% و 66% .
از آنجایی که FLL ممکن است در پارانشیمهای کبدی پسزمینه مختلف رخ دهد، استدلال شد که گزارش نسبتها (نسبت SWV یا نسبت سفتی) بین مقادیر بهدستآمده در FLL و بافت کبد اطراف میتواند دقیقتر باشد.
اگرچه مطالعات فوق امیدوارکننده بودند، اما مطالعات دیگر نتایج کمتر مطلوبی را گزارش کرده اند.
تا به امروز، ارزیابی استفاده برای مشخصههای FLL محدود به نظر میرسد و محدودههای زیادی از مقادیر سفتی برای ضایعات خوشخیم و بدخیم گزارش شده است، با مقادیر HCC SWV از 1.15 m/s (نرم) تا > 4.0 m/s (سفت) در یک مطالعه 58. این تنوع می تواند منعکس کننده ناهمگنی تومور باشد، زیرا گنجاندن خونریزی داخلی یا نکروز در تومورهای بدخیم باعث کاهش سفتی می شود. اگرچه ضایعات خوش خیم به طور کلی نرم تر از ضایعات بدخیم هستند، برخی از ضایعات خوش خیم مانند هیپرپلازی ندولار کانونی (FNH) که عمدتاً از سلول ها و عروق هیپرپلاستیک کبدی تشکیل شده است، دارای سپتوم فیبری و اسکار مرکزی هستند که می تواند سفتی آن را افزایش دهد. قبل از اینکه استفاده از آن برای توصیف ضایعات کانونی کبد توصیه شود، تحقیقات بیشتری لازم است.
مقالات پیشنهادی :
محدودیت های الاستوگرافی سونوگرافی کبد
اندازهگیریهای استفاده از کبد را میتوان با فرآیندهای فیزیولوژیک پاتولوژیک و طبیعی مخدوش کرد (شکل 5). قابل ذکر است، از آنجایی که کبد توسط یک کپسول سفت و با حداقل قابل انبساط (کپسول گلیسون) احاطه شده است، هر گونه افزایش در حجم کبد نیز سفتی آن را افزایش می دهد و اندازه گیری های کشسانی را افزایش می دهد. گزارش شده است که فرآیندهای بیماری از جمله التهاب کبد، احتقان غیرفعال کبد به عنوان مثال در نارسایی قلبی، کلستاز و استئاتوز کبدی بر اندازهگیریهای USE تأثیر میگذارند.
اثرات استئاتوز کبدی بر اندازهگیریهای موج برشی. پتا و همکاران با استفاده از 1D-TE در 253 بیمار مبتلا به بیماری کبد چربی غیرالکلی (NAFLD) با بیوپسی ثابت کردند که درجه استئاتوز یک پیشبینیکننده مستقل برای اندازهگیری سفتی کبد بالاتر است (p = 0.03)، منجر به نرخ مثبت کاذب 23.6٪ در تشخیص می شود فیبروز قابل توجه کبد . یک مطالعه 1D-TE چند مرکزی شامل 650 بیمار مبتلا به HCV مزمن، تأثیر استئاتوز را بر اندازهگیریهای استفاده از سفتی کبد در مقایسه با اندازهگیریهای مورفومتریک کمی و دقیق بافتشناسی کبد بهدستآمده از بیوپسی ارزیابی کرد.
اسلایدهای بافت شناسی بیوپسی کبد برای به دست آوردن تصاویر با کیفیت بالا برای ارزیابی مورفومتری اسکن شدند. آنها دریافتند که 12.6٪ از F0/1 به اشتباه به عنوان F2 طبقه بندی شده است، زمانی که ناحیه استئاتوز نمونه کبد (مساحت وزیکول های استئاتوز در سطح کامل کبد برآورد شده توسط مورفومتری) <4.0٪ بود. زمانی که ناحیه استئاتوز ≥ 4% بود، میزان طبقهبندی اشتباه به 32.4% افزایش یافت. سمیر و همکاران از 2D-SWE (SSI) برای ارزیابی 136 بیمار مبتلا به CLD استفاده کردند و دریافتند که استئاتوز با اندازهگیریهای SWE بهدستآمده در لوب کبد بالا سمت راست (r=0.45، p=0.06)، لوب کبد راست پایین (r) مرتبط نیست. 26/0=، 09/0=p) و محل بیوپسی (04/0=r، 62/0=p) 38. به طور مشابه، وونگ و همکاران هیچ تأثیری از وجود استئاتوز بر اندازهگیریهای سفتی کبد پیدا نکردند (31/0=p) .
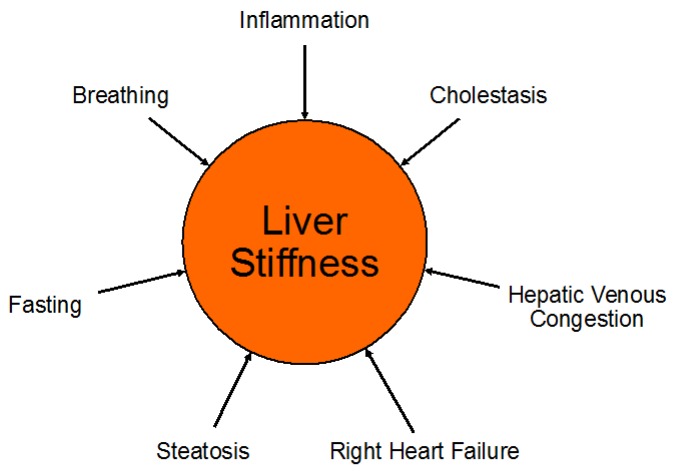
فرآیندهای فیزیولوژیک پاتولوژیک و طبیعی که می توانند عوامل مخدوش کننده اندازه گیری سفتی کبد باشند. در میان علل دیگر، نارسایی قلب راست می تواند منجر به احتقان وریدی کبدی با افزایش متوالی سفتی کبد به دلیل افزایش فشار وریدی شود. افزایش سطوح دم و بازدم (مانور Valsalva) همچنین می تواند سفتی کبد را افزایش دهد و بنابراین، بیماران باید در هنگام اندازه گیری سفتی کبد در مورد دستورالعمل های تنفسی آموزش ببینند.
محدودیت های دیگر مربوط به روش های USE خاص است. از آنجایی که در 1D-TE تحریکات در سطح پوست اعمال می شود، به دلیل چاقی بیمار، فضاهای بین دنده ای باریک و وجود آسیت اطراف کبدی محدود می شود. تصاویر حالت B را ارائه نمی دهد، که می تواند انتخاب یک منطقه نمونه برداری مناسب را محدود کند. این عوامل به نرخ بالای نتایج غیرقابل اعتماد (تقریباً 16٪) با 1D-TE 62 کمک می کنند. روش های جدیدتر از جمله pSWE و 2D-SWE در سیستم های معمولی ایالات متحده موجود هستند و به تجهیزات تخصصی نیاز ندارند. با این حال، تخصص فنی و تشریحی بیشتری با این روش ها مورد نیاز است، بنابراین معمولاً توسط رادیولوژیست یا سونوگرافیک انجام می شود.
در نهایت، از آنجایی که هر دو pSWE و 2D-SWE در مقایسه با 1D-TE فن آوری های جدیدتری هستند، مطالعات اعتبار سنجی بیشتری برای ارزیابی دقت تشخیصی آنها در درجه بندی فیبروز کبدی، پیش بینی واریس های مری، یا شناسایی FLLs 6 مورد نیاز است.
به طور خلاصه، در حالی که کاربرد اصلی بالینی استفاده از کبد شناسایی، مرحله بندی و نظارت بر فیبروز کبدی در بیماران CLD است، دستورالعمل های فدراسیون جهانی اولتراسوند در پزشکی و زیست شناسی (WFUMB) تنها استفاده از آن را در تشخیص (F≥2) مهم توصیه می کند. یا فیبروز پیشرفته (F≥3) از فیبروز غیر قابل توجه (F0-F1) به دلیل محدودیت های فعلی USE در تمایز بین مراحل فیبروز فردی 18. به طور مشابه، انجمن رادیولوژیست ها در بیانیه کنفرانس اجماع اولتراسوند، استفاده از کبد را برای تمایز بیماران مبتلا به فیبروز توصیه می کند. یا حداقل فیبروز (F0-F1) از مبتلایان به فیبروز شدید یا سیروز (F3-F4). کار آینده برای بهبود کاربرد کبدی شامل پیشرفتهای فنی برای افزایش دقت تمایز بین مراحل فیبروز و استانداردسازی تکنیکهای الاستوگرافی در بین فروشندگان میشود.
مقالات پیشنهادی :
اکوکاردیوگرافی قلب جنین
پستان
سرطان پستان شایعترین بدخیمی در ایالات متحده برای زنان است که طبق اعلام موسسه ملی سرطان، تقریباً 12.3 درصد در طول عمر تشخیص داده میشود. تشخیص زودهنگام سرطان سینه از طریق تست های غربالگری امکان درمان کامل را فراهم می کند .
دو روش متداول تصویربرداری برای غربالگری سرطان پستان ماموگرافی و US هستند. با این حال، هر دو محدودیتهایی دارند، مانند نتایج منفی کاذب در ارزیابی ماموگرافی سینههای متراکم و ویژگی ضعیف B-mode US 63. USE یک ابزار مکمل برای بهبود خصوصیات غیرتهاجمی ضایعات پستان فراهم میکند.
مطالعات نشان داده اند که استفاده از پستان نتایج مطلوبی را در مقایسه با حالت B و ماموگرافی دارد. برای مثال، مطالعه اخیری که SE USE را با B-mode US و ماموگرافی مقایسه کرد (114 ضایعه کل، 33 ضایعه بدخیم تایید شده توسط بافت شناسی) نشان داد که USE خاص ترین روش در بین 3 روش بود (ویژگی = 95.1%). . در مطالعه ای توسط فیشر و همکاران در مقایسه SE USE با B-mode US و ماموگرافی (116 ضایعه بدخیم هیستولوژیکی اثبات شده)، حساسیت (95%) و ویژگی (74%) USE نیز بیشتر از ماموگرافی و B-mode US 65 بود. با توجه به بهبود تشخیصی با نتایج USE، اضافه شدن USE به حالت B و ماموگرافی میتواند به رادیولوژیستها کمک کند تا مناسبترین دسته طبقهبندی گزارشدهی و دادههای تصویربرداری پستان (BI-RADS) را برای راهنمایی مدیریت انتخاب کنند. اخیراً، اندازهگیریهای کیفی الاستیسیته USE (نرم، متوسط یا سخت) ضایعات پستان به عنوان یک یافته مرتبط در ویرایش دوم واژهنامه BI-RADS US گنجانده شده است.
تصویربرداری کرنش در ضایعات پستان
پارامترهای متعددی برای توصیف توده های خوش خیم و بدخیم پستان با تصویربرداری کرنش استفاده شده است. رایج ترین پارامترها امتیاز Tsukuba (امتیاز کشش)، نسبت حالت EI/B (نسبت عرض یا نسبت طول) و نسبت کرنش (نسبت چربی به ضایعه FLR) است.
امتیاز Tsukuba (یک مقیاس رنگی پنج نقطه ای) بر اساس نقشه سفتی بافت در داخل و اطراف ضایعه است که در آن امتیاز بر اساس سفتی ضایعه نسبت به سفتی بافت زمینه محاسبه می شود. همانطور که در شکل 6 نشان داده شده است. نمرات Tsukuba به این صورت اختصاص داده می شود: 1) ضایعه کمتر یا مساوی سفتی بافت اطراف است. 2) ضایعه دارای مناطق سفتی مخلوط (افزایش، کاهش یا مساوی) نسبت به بافت های اطراف است. 3) ضایعه سفت تر از بافت اطراف است و اندازه آن در الاستوگرام نسبت به B-mode US کوچکتر است. 4) ضایعه سفت تر از بافت اطراف است و در الاستوگرام و B-mode US هم اندازه است. و 5) ضایعه سفت تر از بافت اطراف است و از نظر اندازه در الاستوگرام بزرگتر از B-mode US 67 است. نمرات بالاتر با احتمال بیشتر بدخیمی مطابقت دارد، با نمرات 1-3 نشان دهنده یک ضایعه احتمالاً خوش خیم و امتیاز 4 است. -5 نیاز به بیوپسی دارد.
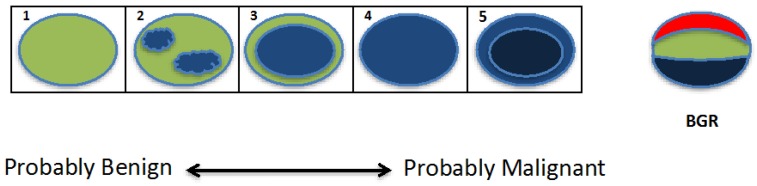
نمایش گرافیکی امتیاز تسوکوبا. ضایعه به صورت بیضی شکل نشان داده می شود و رنگ ها نشان دهنده سفتی ضایعه (آبی=افزایش یافته، قرمز=کاهش) در مقایسه با بافت اطراف است. با افزایش نمره تسوکوبا (1-5)، ضایعات احتمال بدخیمی بالاتری دارند. ظاهر سه لایه نوارهای آبی، سبز و قرمز (BGR) (تصویر سمت راست) تشخیص کیست است که با استفاده از چندین فروشنده اولتراسوند (مانند هیتاچی، توشیبا) تجسم شود (شکل اقتباس شده از Itoh et al, 2006 9).
امتیاز Tsukuba به طور گسترده ای برای افتراق بین ضایعات خوش خیم و بدخیم پستان استفاده شده است. برای مثال، Itoh و همکاران. نشان داد که امتیاز تسوکوبا دارای حساسیت، ویژگی و دقت به ترتیب 5/86، 9/89 و 3/88 درصد است. 83% و میانگین ویژگی برای تشخیص ضایعات بدخیم پستان 84% بود. به طور کلی با افزایش ویژگی (68.3٪ به 87.8٪) و کمی کاهش حساسیت (90.3٪ به 83.9٪) بهبود یافت.
در نسبت EI/B-mode، اندازه ضایعه اندازه گیری شده در الاستوگرام بر اندازه ضایعه اندازه گیری شده در B-mode US تقسیم می شود. این نسبت از این یافته استفاده می کند که قطر عرضی یک ضایعه خوش خیم در یک الاستوگرام کوچکتر از حالت B-mode مربوطه است. برعکس، قطر عرضی یک ضایعه بدخیم در الاستوگرام بزرگتر از حالت B است زیرا پاسخ استرومایی به سرطان سینه هم سفتی تومورها و هم بافت های اطراف را افزایش می دهد. اعتبار نسبت EI/B-mode توسط یک مطالعه نشان داده شده است که 54 ضایعه بدخیم پستان را از نظر بافت شناسی با استفاده از برش نسبت EI/B-mode ≥ 1.0 به عنوان بدخیم و <1.0 به عنوان خوش خیم ارزیابی کرد. این مطالعه حساسیت و ویژگی عالی (به ترتیب 100 و 95 درصد) را در افتراق ضایعات بدخیم از خوش خیم پستان نشان داد.
نسبت کرنش، نسبت کرنش در یک توده به سویه در چربی زیر جلدی است. از آنجایی که چربی مدول الاستیک ثابتی بر روی فشارهای مختلف دارد، این نسبت یک اندازه گیری نیمه کمی است که نشان دهنده سفتی نسبی ضایعه است.
مقالات پیشنهادی :
هر دو نسبت EI/B-mode و نسبت کرنش به طور گسترده مورد مطالعه قرار گرفته اند، همانطور که توسط یک متاآنالیز نشان داده شده است که شامل 12 مطالعه USE است که نسبت کرنش (9 مطالعه، 2087 ضایعه پستان) یا نسبت EI/B-mode را گزارش می کند (3 مطالعه، 450 ضایعات پستان) برای توصیف ضایعات کانونی پستان . حساسیت و ویژگی تلفیقی برای مطالعات نسبت کرنش (به ترتیب 88٪، 83٪) و مطالعات نسبت EI/B-mode (به ترتیب 98٪، 72٪) خوب بود (جدول .
تصویربرداری موج برشی در ضایعات پستان
در SWI، یک اندازه گیری کمی از سرعت موج برشی (m/sec) یا مدول یانگ (kPa) در یک ضایعه یا به عنوان یک مقدار واحد در یک ناحیه کوچک ثابت مورد علاقه (ROI) یا برای هر پیکسل در یک میدان به دست می آید. کادر نمای (FOV) به صورت نقشه رنگی 19، 67 نمایش داده میشود. معمولاً از مقیاس رنگی از 0 (آبی تیره = نرم) تا 180 کیلو پاسکال (قرمز = سخت) در سینه USE 73 استفاده میشود (شکل 7).
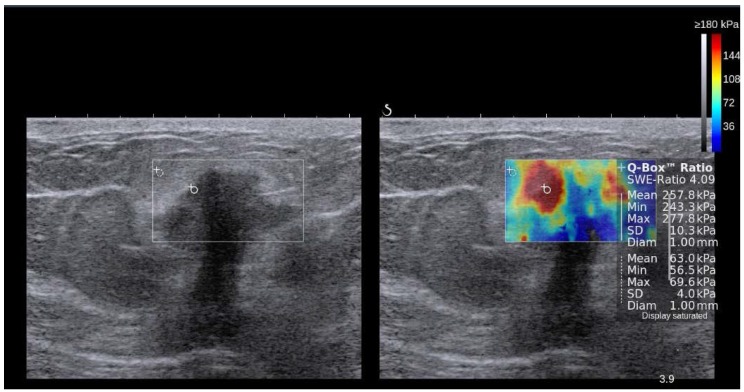
نمایش کنار هم از تصویر آناتومیک B-mode ایالات متحده (سمت چپ) و نقشه رنگی روکش شده از اندازه گیری امواج برشی همزمان (سمت راست) یک ضایعه پستان که با 2D-SWE در SuperSonic Imagine (SSI) AixplorerTM به دست آمده است. در این سیستم رنگ قرمز نشان دهنده بافت سفت و رنگ آبی نشان دهنده بافت نرم است. ضایعه هیپواکوئیک مشکوک (در داخل مستطیل در تصویر حالت B نشان داده شده است) دارای حاشیه نامنظم، حاشیه های زاویه ای، کمی پهن تر از ارتفاع است و سایه های آکوستیک خلفی را نشان می دهد. الاستوگرام اتیولوژی بدخیم را به دلیل افزایش سفتی (قرمز/زرد/سبز) پیشنهاد کرد و آدنوکارسینوم مجرای در بیوپسی بعدی تایید شد. تصویر توسط دکتر اسمار سایتو.
چندین مطالعه استفاده از SWI را برای مشخص کردن ضایعات پستان تایید کردهاند (جدول (جدول 3). در یک متاآنالیز اخیر از 11 مطالعه SWI که ضایعات پستان را ارزیابی می کرد (2424 بیمار)، مقادیر کمی کشسانی، از جمله میانگین سفتی و حداکثر سفتی، رایج ترین پارامترهای مورد استفاده، به دست آمد. در این متاآنالیز، حساسیتها و ویژگیهای تلفیقی خوب برای SWI بر اساس حداکثر سختی (به ترتیب 93٪، 81٪) و میانگین سختی (به ترتیب 94٪، 71٪) نشان داده شد. یک مطالعه دیگر SWI روی 83 ضایعه پستان، حساسیت و ویژگی مشابهی را به ترتیب 94% و 73% پیدا کرد .
مقالات پیشنهادی :
چندین مطالعه همچنین ارزیابی کردند که آیا افزودن SWI میتواند عملکرد B-mode US را در ارزیابی بدخیمی پستان بهبود بخشد . به عنوان مثال، فلدمن و همکاران. از پارامترهای کیفی (ظاهر همگن یا ناهمگن) و کمی (اندازه، مقادیر سفتی (E) و مقادیر نسبت (R)) 2D-SWE علاوه بر B-mode US برای تمایز بین ضایعات بدخیم و خوش خیم پستان استفاده کرد. متمایزترین ویژگی های 2D-SWE ظاهر روی نقشه رنگی SWE و مقدار نسبت اطراف ضایعه (Rperilesion) با آستانه 4.32 بود. Rperilesion سخت ترین بخش ناحیه اطراف ضایعه (Eperilesion) و نرم ترین بافت چربی سالم (Efat) را از طریق نسبت: Rperilesion = Eperilesion / Efat ارزیابی می کند. آنها نشان دادند که با استفاده از علائم خوش خیم SWI (همگنی و Rperilesion < 4.32)، برای کاهش انتخابی ضایعات B-mode طبقه بندی شده ایالات متحده BI-RADS 4a (ظن کم بدخیمی) و BI-RADS 4b (ظن متوسط برای بدخیمی) ضایعات ایالات متحده (ویژگی ایالات متحده را بهبود بخشید). 13٪ تا 51٪ بدون از دست دادن حساسیت (100٪) . برگ و همکاران مطالعه ای را با 958 زن با ضایعات سینه انجام دادند که نشان داد SWI ویژگی B-mode US را بهبود بخشید. 61.1٪ تا 78.5٪ . بنابراین، اگر ضایعه طبقه بندی شده به عنوان BI-RADS 4a دارای ویژگی های SWI خوش خیم باشد، می توان آن را به BI-RADS 3 (احتمالاً خوش خیم) کاهش داد، که موارد زیر را تضمین می کند. این روش نویدبخش بهبود مدیریت بیمار و کاهش بیوپسیهای غیرضروری است، اما مطالعات بیشتری برای اعتبارسنجی بیشتر ضروری است.
محدودیت های الاستوگرافی سونوگرافی پستان
محدودیت های زیر برجسته شده است:
- کدگذاری رنگ و امتیازدهی الاستوگرام استاندارد نشده است .
- گاهی اوقات یک ضایعه بدخیم ممکن است در SWI نرم به نظر برسد. سپس بافت های اطراف باید به دقت مورد مطالعه قرار گیرند تا به شناسایی سفت ترین قسمت ضایعه کمک کند. افزایش سرعت موج برشی در بافت های اطراف برای کمک به توصیف ضایعه به عنوان بدخیم مرتبط است.
- مشخص کردن ضایعات ناهمگن با ویژگی های مخلوط خوش خیم (کیستیک) و بدخیم (نکروز) دشوار است.
- برخی از ضایعات خوش خیم (مانند فیبروآدنوم هیالینیزه، فیبروز و نکروز چربی) نیز ممکن است سفت باشند.
- ارزیابی توده ها در پستان خلفی دشوار است زیرا بافت های عمیق ممکن است توسط نیروهای فشاری اعمال شده در سطح سینه جابجا نشوند.
مقالات پیشنهادی :
به طور خلاصه، کاربردهای فعلی الاستوگرافی سونوگرافی بالینی پستان در دستورالعملهای اخیر WFUMB برجسته شده است، که بیان میکند که تصویربرداری از فشار یا SWI فقط باید در ارتباط با B-mode US برای توصیف یک ناهنجاری شناسایی شده در حالت B انجام و تفسیر شود. با توجه به این توصیه ها، معقول است که ضایعات با کشش نرم که BI-RADS 3 هستند (معیارها: نمره 1 در تصویربرداری کرنش، یا حداکثر رنگ آبی تیره یا حداکثر کشش ≤ 20 کیلو پاسکال در SWI) 73 یا BI کاهش یابد. -RADS 4A (معیارها: امتیاز 1 یا 2 در تصویربرداری کرنش و حداکثر الاستیسیته رنگ آبی روشن یا حداکثر کشش ≤ 80 کیلو پاسکال در SWI برای یک استراتژی تهاجمی، و امتیاز 1 در تصویربرداری کرنش و حداکثر رنگ الاستیسیته آبی تیره یا حداکثر کشش ≤30 کیلو پاسکال در SWI برای یک استراتژی محافظه کارانه) 76. اگر ضایعه BI-RADS 3 دارای ویژگی های بدخیمی در SE یا SWI باشد (E Max> 160 kPa (7.3 m/s) یا E Color= قرمز با مقیاس SWI که روی 180 کیلو پاسکال (7.7 متر بر ثانیه) تنظیم شده است، باید به بیوپسی ارتقا یابد.
با این حال، هنوز کار زیادی برای حمایت از کاربردهای بالینی فعلی استفاده از پستان وجود دارد. به عنوان مثال، در حالی که هر دو تصویربرداری از سویه و SWI میتوانند خصوصیات تودههای پستان را بهبود بخشند، هیچ مطالعه مقایسهای برای نشان دادن برتری یک روش بر روش دیگر انجام نشده است. این امکان وجود دارد که استفاده از بیش از یک روش USE در یک زمان بر روی یک بیمار اعتماد به یافتهها را بهبود بخشد. ارزیابی عملکرد تشخیصی USE در ضایعات با اندازههای مختلف و در اعماق بافت پستان مختلف هنگام استفاده در ترکیب با B-mode US 71.
تیروئید
ندول های تیروئید یک یافته رایج در جمعیت عمومی است که در 67% بزرگسالان با وضوح بالا با حالت B و در 50% از معاینات پاتولوژیک در کالبد شکافی وجود دارد. تشخیص زیر مجموعه تیروئید مهم است. ندولهایی که بدخیم هستند، زیرا عوارض و مرگ و میر ناشی از سرطان تیروئید با مرحله بیماری افزایش مییابد. علیرغم شیوع بالای ندول های تیروئید، تنها 8-4 درصد از ندول های نمونه برداری شده توسط آسپیراسیون با سوزن ظریف (FNA) بدخیم هستند. ویژگی هایی مانند لبه های دایره ای، شکل بلندتر از پهن، هیپواکوژنیسیته مشخص و میکروکلسیفیکاسیون ها حاکی از بدخیمی هستند. سپس FNA معمولاً برای تأیید بدخیمی استفاده می شود.
اگرچه FNA استاندارد طلایی برای تشخیص در نظر گرفته میشود، اما هنوز ناقص است، زیرا 15 تا 30 درصد نمونهها غیرتشخیصی یا نامشخص در نظر گرفته میشوند. نتایج دوباره برای 9.9-50٪ از گره ها با سیتولوژی غیر تشخیصی اولیه و 38.5-43٪ از ندول ها با سیتولوژی نامشخص اولیه به دست آمده است. به دلیل معضل نئوپلاسمهای فولیکولی که به راحتی قابل اصلاح نیستند، میتوانند 6.7 درصد از کل نتایج FNA یا 22 درصد از نتایج FNA غیرقطعی را شامل شود. تعیین با FNA، بیوپسی هسته یا حتی تجزیه و تحلیل بخش منجمد دشوار است.
الاستوگرافی سونوگرافی تیروئید یک روش غیر تهاجمی برای ارزیابی گره های تیروئید است که اطلاعات تکمیلی برای US و FNA حالت B ارائه می دهد. استفاده ترکیبی از تیروئید USE با B-mode US ممکن است توانایی تشخیص ندول های خوش خیم از بدخیم تیروئید را بهبود بخشد و تعداد FNA های مورد نیاز را کاهش دهد. استفاده از تیروئید ممکن است به مشکل دشوار تمایز بین نئوپلاسم های فولیکولی بدخیم و خوش خیم کمک کند.
تصویربرداری از فشار سونوگرافی تیروئید
مطالعات تصویربرداری فشار اولتراسوند تیروئید را می توان بر اساس انواع محرک ها و سیستم های امتیازدهی طبقه بندی کرد. رایج ترین محرک مورد استفاده در تصویربرداری کرنش اولتراسوند تیروئید، فشرده سازی خارجی اعمال شده توسط اپراتور از طریق مبدل اولتراسوند است (شکل 8.8). روش دیگر، محرک فیزیولوژیکی با استفاده از ضربانهای شریان کاروتید برای القای حرکت غده تیروئید مجاور با نتایج دلگرمکننده مورد مطالعه قرار گرفته است. الاستوگرافی سونوگرافی پستان، 84 یا معیار راگو، امتیاز 5 امتیازی 86) و شاخص سفتی تیروئید نیمه کمی (کرنش در پس زمینه تیروئید نرمال / فشار در ندول تیروئید) . معیار آستریا بر اساس چهار دسته از سفتی بافت: امتیاز 1 برای گره های نرم. امتیاز 2 و 3 برای گره هایی با درجه سفتی متوسط. نمره 4 برای ضایعات سفت . به طور مشابه، معیار راگو از نمره 1 (یکنواخت کشسانی در کل ندول) تا نمره 5 (بدون کشش در ندول یا در ناحیه ای که سایه های خلفی را نشان می دهد) متغیر است.
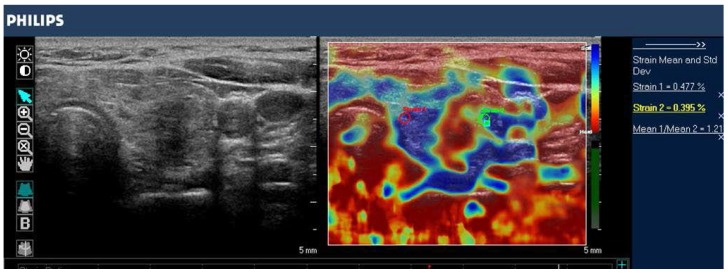
تصویر حالت B (سمت چپ) و الاستوگرام با کد رنگی (راست) از یک گره تیروئید در غده تیروئید چپ، با SE در سیستم فیلیپس iU22 تصویر شده است. ندول هیپواکویک با مرزهای نامشخص در تصویر آناتومیک حالت B به نظر می رسد. الاستوگرام بافت نرمال تیروئید را با رنگ آبی (بافت نرم) و ندول را با رنگ قرمز (بافت سفت) نشان می دهد که نشان دهنده ندول بدخیم است. این مورد توسط بافت شناسی که کارسینوم پاپیلاری تیروئید را نشان می داد تایید شد.
مطالعات با استفاده از تصویربرداری فشار اولتراسوند برای ارزیابی گرههای تیروئید نتایج متفاوتی را نشان دادهاند . یک متاآنالیز شامل 639 گره تیروئید نشان داد که تصویربرداری از سویه برای ارزیابی بدخیمی مفید است، با میانگین کلی حساسیت 92 درصد و میانگین ویژگی 90 درصد . این یافته ها با نتایج یک مطالعه گذشته نگر اخیر با 703 گره، که نشان داد حساسیت اندازهگیریهای تصویربرداری کرنش (15.7٪ معیارهای 5 نقطهای راگو، 65.4٪ معیارهای 4 نقطهای Asteria) کمتر از ویژگیهای B-mode US (91.7٪) بود . اخیراً، یک مطالعه آینده نگر با 912 ندول نشان داد که تصویربرداری از سویه نسبت به ویژگی های B-mode ایالات متحده در پیش بینی بدخیمی، با حساسیت 80.2٪ و ویژگی 70.3٪ برتری دارد.
از آنجایی که حالت B-US و تصویربرداری سویه معیارهای مستقلی را ارائه میدهند، فرض بر این است که ترکیب اندازهگیریها برای ارزیابی بدخیمی برتر از هر یک به تنهایی است. این توسط نتایج Trimboli و همکاران پشتیبانی شد، که در آن ترکیب دو روش منجر به حساسیت 97٪ و ارزش اخباری منفی 97٪ شد که بالاتر از استفاده از SI به تنهایی است (حساسیت = 81٪، ارزش اخباری منفی = 91٪ یا ویژگی های حالت B به تنهایی (حساسیت = 85٪، ارزش اخباری منفی = 91٪) 91. در مقابل، مون و همکاران دریافتند که ترکیب اندازه گیری های SI و ویژگی های B-mode US نسبت به استفاده از ویژگی های حالت B پایین تر است.
این نتایج مختلط از مطالعات تصویربرداری فشار اولتراسوند تیروئید ممکن است به دلیل جمعیت های مختلف و معیارهای خروج مورد استفاده در مطالعات مختلف باشد. به طور خاص، درصد ندولهای بدخیم تیروئید بین مطالعات متفاوت است و از 9.4 درصد در عزیزی و همکاران 90 تا 31 درصد در مون و همکاران 89 متغیر است. مطالعات آیندهنگر بیشتری با اندازه کوهورت بزرگتر برای ارزیابی ارزش بالینی تصویربرداری کرنش در توصیف تیروئید مورد نیاز است. ندول ها
تصویربرداری امواج برشی تیروئید
برخلاف تصویربرداری کرنش، SWI گره های تیروئید اندازه گیری های کمی را ارائه می دهد (شکل 9). تعدادی از متاآنالیزهای اخیر SWI نتایج امیدوارکنندهای را در 92-95 نشان دادهاند، با شباهتهای بین نتایج حداقل تا حدی به دلیل همپوشانی قابلتوجه در مطالعات وارد شده. Zhan و همکاران شامل مطالعات pSWE و بزرگترین متاآنالیز (2436 گره تیروئید) بودند. آنها دریافتند که pSWE برای افتراق ندول های خوش خیم از بدخیم مفید است (میانگین حساسیت = 80٪، میانگین ویژگی = 85٪، جدول 3) 3) 92. متاآنالیز توسط Dong و همکاران همچنین شامل مطالعات pSWE بود و نتایج مشابه خوبی پیدا کرد. 1617 ندول تیروئید، حساسیت تلفیقی = 86.3٪، ویژگی تلفیقی = 89.5٪
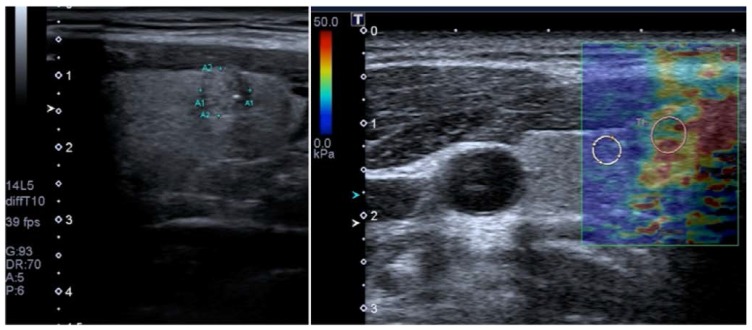
تصویر حالت B عرضی (سمت چپ) ندول ناهمگن تیروئید کوچک (ضایعه در ناحیه مورد نظر) با حاشیه های نامشخص و میکروکلسیفیکاسیون در لوب تیروئید راست را نشان می دهد که نشان دهنده علت بدخیم است. الاستوگرام رنگی مربوطه به دست آمده با 2D-SWE روی توشیبا آپلیو 500 (سمت راست) سفتی افزایش یافته ندول (ROI صورتی؛ 32.7 کیلو پاسکال) را در مقایسه با پارانشیم طبیعی اطراف (ROI سفید؛ 7.4 کیلو پاسکال) نشان می دهد که نشان می دهد ندول بدخیم است. بیوپسی بعدی کارسینوم پاپیلاری را تایید کرد.
یک مطالعه آینده نگر اخیر به طور خاص به این سؤال پرداخته است که آیا 2D-SWE می تواند بین نئوپلاسم های فولیکولی خوش خیم و بدخیم تیروئید تمایز قائل شود . در این کار، 35 بیمار با گره های تیروئیدی که تشخیص FNA نئوپلاسم های فولیکولی داشتند. قبل از عمل جراحی با B-mode US و 2D-SWE مورد ارزیابی قرار گرفتند. اگرچه ویژگی های B-mode US پیش بینی کننده بدخیمی فولیکولی نبودند، برآورد مدول یانگ بالاتر با بدخیمی فولیکولی مرتبط بود (AUC = 0.81، مقدار برش = 22.3 kPa، حساسیت = 82٪، ویژگی = 88٪، ارزش اخباری مثبت = 75٪، ارزش اخباری منفی = 91٪ 78.
تعداد فزاینده مطالعات SWI ندول تیروئید به طور کلی نتایج دلگرم کننده ای ارائه کرده است. این یافته که SWI ممکن است برای تشخیص دشوار و در نتیجه مدیریت بالینی بدخیمی در نئوپلاسم های فولیکولی مفید باشد، به ویژه هیجان انگیز است. اگر بدخیمی نئوپلاسمهای فولیکولی قبل از جراحی بهتر ارزیابی میشد، میتوان همی تیروئیدکتومی را ترجیحاً برای نئوپلاسمهای خوشخیم فولیکولی انجام داد و بیماران را از تعهد جایگزینی هورمون تیروئید در طول عمر از یک تیروئیدکتومی کامل غیرضروری نجات داد.
محدودیت های الاستوگرافی سونوگرافی تیروئید
مقالات پیشنهادی :
محدودیت های زیر در مطالعات برجسته شده است:
- فشرده سازی خارجی دستی در تصویربرداری کرنش منجر به تغییرپذیری وابسته به اپراتور 96 می شود.
- غیر خطی بودن سفتی بافت منجر به اندازه گیری سفتی بیشتر در درجات فشرده سازی 96 می شود.
- فیبروز درون ندول های خوش خیم و بدخیم می تواند سفتی را افزایش دهد.
- بسیاری از مطالعات قبلی به دلیل اندازه کوهورت کوچک با سوگیری انتخاب بیمار و فقدان تکنیک استاندارد شده (مقیاس رنگ الاستوگرام، مقادیر برش) محدود شده اند.
- ندول های تیروئید با قطر بیشتر از 3 سانتی متر ممکن است نتوانند به اندازه کافی در تصویربرداری سویه فشرده شوند.
- الاستوگرافی اولتراسوند اطلاعات معنی داری را با گره هایی که دارای اجزای کیستیک هستند نمی دهد، زیرا حرکت مایع نشان دهنده سفتی جزء جامد مورد نظر نیست.
- الاستوگرافی اولتراسوند را نمی توان بر روی گره هایی با پوسته کلسیفیه انجام داد زیرا امواج صوتی به کلسیفیکاسیون ها نفوذ نمی کند تا قسمت مرکزی غیر کلسیفیه مورد نظر را ارزیابی کند.
- کلسیفیکاسیون درشت در ندول های خوش خیم تیروئید می تواند منجر به اندازه گیری های گمراه کننده شود که نشان دهنده افزایش سفتی است که در غیر این صورت مشخصه بدخیمی 84 خواهد بود.
به طور خلاصه، نتایج با استفاده از الاستوگرافی اولتراسوند برای تشخیص ندولهای خوشخیم از بدخیم تیروئید، به طور کلی دلگرمکننده هستند و اطلاعات تکمیلی غیرتهاجمی را برای B-mode US ارائه میدهند. حتی یک مطالعه نشان میدهد که تصویربرداری موج برشی ممکن است به تشخیص بدخیمی فولیکولی کمک کند، زمانی که نتایج FNA تهاجمی نامشخص هستند. سیستم های امتیاز دهی (به عنوان مثال امتیاز کشش 4 یا 5 امتیاز، شاخص سفتی). برای اینکه این نتایج اولیه امیدوارکننده کاربرد بالینی گسترده ای به دست آورند، اعتبار سنجی بیشتر با مطالعات آینده نگر کوهورت بزرگ و استانداردسازی تکنیک ها ضروری است.
اصول اولتراسوند
الاستوگرافی سونوگرافی آندوسکوپی
الاستوگرافی یک روش مبتنی بر اولتراسوند برای ارزیابی "سختی" بافت (یعنی تغییر در ابعاد بافت [کرنش] ناشی از نیروی اعمال شده) است. این مفهوم ارتباط نزدیکی با لمس دارد، که پزشکان قرن ها از آن برای تشخیص آسیب شناسی مرتبط با "سفتی" بافت بالاتر استفاده می کردند. پارامترهای متعددی وجود دارد که خواص کشسانی بافت را توصیف می کند، از جمله مدول توده ، که تغییر حجم ماده را در پاسخ به تنش خارجی توصیف می کند. مدول حجیم تنها بیش از 15٪ در بین انواع مختلف بافت متفاوت است. با این حال، لمس پارامترهای کشش متفاوتی را ایجاد می کند - مدول یانگ و / یا مدول برشی، که نشان دهنده نسبت جابجایی (یا کرنش) بافت در یک جهت خاص (طولی یا عرضی) به تنش اعمال شده است. مدول الاستیک بافت نرم طبیعی به اندازه چهار مرتبه بزرگی متفاوت است و در اثر تغییرات پاتولوژیک مانند فیبروز تا دو مرتبه بزرگتر می شود، در حالی که تومورهای خوش خیم عموماً نرم تر از تومورهای بدخیم هستند.
سونوگرافی و الاستوگرافی با کنتراست تقویت شده
الاستوگرافی اولتراسوند و سونوگرافی با کنتراست تقویت شده (CEUS) تکنیک های پیشرفته ای برای مشخص کردن ندول تیروئید هستند که در دهه گذشته تحقیقات زیادی انجام شده است. CEUS ممکن است ماکروواسکولاریزاسیون و میکروواسکولاریزاسیون ندولهای تیروئید را به تصویر بکشد و ارزیابی کیفی و کمی را ارائه دهد. ندول ها بسته به بافت شناسی افزایش ناهمگنی را نشان می دهند. ندول های بدخیم اغلب افزایش کنتراست ایزوهیپوواسکولار و تخلیه کندتر نسبت به پارانشیم تیروئید دارند، در حالی که ندول های خوش خیم افزایش بیش از حد عروقی و الگوی لبه مانند را نشان می دهند. حساسیت، ویژگی و نسبت احتمال مثبت و منفی (LR) به ترتیب 0.853، 0.876، 5.822 و 0.195 برای افتراق ندول های خوش خیم از بدخیم دقیق است، 85 اما مطالعات با حجم نمونه بزرگتر برای تایید این داده های اولیه مورد نیاز است.
همچنین از الاستوگرافی برای مطالعه گره های تیروئید استفاده شده است. الاستوگرافی اطلاعاتی در مورد خاصیت ارتجاعی بافت ارائه می دهد، بر اساس این فرض که فرآیندهای پاتولوژیک مانند سرطان ویژگی های فیزیکی بافت درگیر را تغییر می دهند. هدف تهیه دو تصویر سونوگرافی (قبل و بعد از فشرده سازی بافت) و ردیابی جابجایی بافت با ارزیابی انتشار پرتو است که اندازه گیری دقیق اعوجاج بافت را فراهم می کند.
الاستوگرافی که بر روی غده تیروئید اعمال می شود، با توجه به نوع نیروی فشاری (تحریک) و ارزیابی الاستیسیته، اصولاً از دو رویکرد متفاوت استفاده می کند: (1) الاستوگرافی فشاری سونوگرافی آزاد، با کیفی آن (بر اساس نقشه های رنگ سنجی و تقسیم به چهار یا پنج کلاس)88 و انواع نیمه کمی (مقدار نسبت کرنش). و (2) رویکرد کمی با پالس صوتی بالا ناشی از مبدل و اندازه گیری سرعت موج برشی تولید شده (الاستوگرافی موج برشی [SWE]). SWE را می توان با استفاده از فناوری تکانه نیروی تابش صوتی (ARFI) یا در یک منطقه کوچک مورد علاقه (ROI) (الاستوگرافی موج برشی نقطه ای، p-SWE) یا در یک میدان دید بزرگتر با استفاده از کد رنگی برای نمایش بصری سختی انجام داد. مقادیر (الاستوگرافی موج برشی دو بعدی [2D-SWE]). یک نوع نیمه کمی اضافی از الاستوگرافی فشاری از ضربان داخلی (فیزیولوژیک) شریان کاروتید (الاستوگرافی شبه استاتیک in vivo) استفاده می کند. در این رویکرد، نیازی به فشار خارجی نیست و ضربانهای شریان کاروتید، جابجایی لازم برای ارزیابی کشسانی بافت را القا میکند.
چهار الگوی الاستوگرافی طبقه بندی شده است:
الگوی 1: کشش در کل گره
الگوی 2: خاصیت ارتجاعی در بخش بزرگی از ندول، با ظاهر ناپایدار نواحی بیالاستیک
الگوی 3: حضور دائمی مناطق غیرکشسان بزرگ در حاشیه
الگوی 4: یکنواخت غیر کشسان
EUS با الاستوگرافی
الاستوگرافی کمکی به EUS است که امکان ارزیابی و اندازه گیری کشسانی بافت را فراهم می کند. غدد لنفاوی بدخیم و تومورها نسبت به غدد لنفاوی و بافت های خوش خیم سفت تر و انعطاف پذیرتر هستند. با این حال، همپوشانی شناخته شده ای با فرآیندهای التهابی وجود دارد. این فناوری بر اساس تشخیص تغییر شکل های ساختاری کوچک در تصویر حالت B ناشی از فشرده سازی است. درجه تغییر شکل (حرکت لکه) به عنوان شاخصی برای سفتی بافت استفاده می شود.181 نرم افزار فعلی اجازه می دهد تا یک نقشه رنگی از ضایعه، با توجه به خاصیت ارتجاعی (آبی محکم تا قرمز ملایم)، و بنابراین یکنواختی، یا الگوی در صورت وجود ناهمگن، "سفتی" بافت نیز می تواند ارزیابی شود.
یک مطالعه آزمایشی آلمانی روی 20 فرد عادی، 20 بیمار مبتلا به پانکراتیت مزمن، و 33 بیمار با توده های کانونی پانکراس نشان داد که الاستوگرافی همپوشانی فوق العاده ای بین پانکراتیت مزمن و تومورها دارد. فیبروز باید سفت تر از پانکراس طبیعی باشد. با این حال، اگرچه یافته ها به طور رسمی ارزیابی نشدند، محققان بر این باور بودند که الاستوگرافی در تشخیص پانکراتیت طبیعی از پانکراتیت مزمن مفید به نظر نمی رسد، مگر در موارد پیشرفته تر. یک مطالعه اروپایی چند مرکزی از الاستوگرافی در 222 بیمار هیچ بهبودی در حساسیت نسبت به EUS معمولی نشان نداد اما بهبود کمی در ویژگی (80٪ در مقابل 69٪) نشان داد.
محدودیتهای اصلی الاستوگرافی در تمایز التهاب از نئوپلازی این است که همه تومورها سفت یا سفت نیستند و پانکراتیت کانونی مزمن میتواند بسیار سخت باشد. الگوی الاستوگرافی علاوه بر این، کد گذاری رنگی تصویر توسط نرم افزار در رابطه با سایر بافت های موجود در قاب تصویر انجام می شود و به سفتی بافت شناخته شده "کالیبره" نمی شود. نرم افزار سعی می کند از طیف رنگی کامل استفاده کند حتی اگر ضایعه وجود داشته باشد. همگن نرم یا همگن سفت. بنابراین، رگ های خونی و سایر ساختارهای موجود در میدان ممکن است بر طیف رنگی استفاده شده یا رنگ اختصاص داده شده به قسمت خاصی از تصویر تأثیر بگذارند.
مقالات پیشنهادی :
تکنیک های جدید اولتراسوند: الاستوگرافی
الاستوگرافی اولتراسونیک از تصویربرداری اولتراسوند برای اندازه گیری فشار بافت نرم استفاده می کند تا به طور عینی خواص مکانیکی بافت ها مانند سختی یا سفتی را ارزیابی کند. چندین روش الاستوگرافی اولتراسونیک برای مشخص کردن بافت ها در کاربردهای تحقیقاتی و بالینی (کبد، تودههای سینه و غیره) استفاده شده است و الاستوگرافی به عنوان یک روش تشخیصی اضافی برای شناسایی ترومبوز وریدی مورد مطالعه قرار گرفته است.
الاستیسیته تمایل یک ماده برای از سرگیری اندازه و شکل اولیه خود پس از تغییر شکل توسط یک نیرو است. سیالات فقط دارای خاصیت ارتجاعی حجمی هستند، در برابر تغییرات حجم مقاومت می کنند، اما نه شکل. جامدات در برابر تغییرات شکل و حجم مقاومت می کنند، زیرا هم دارای کشش برشی (سفتی) و هم کشش حجمی هستند. کرنش اصطلاحی است که تغییرات اندازه یا شکل را توصیف می کند. نیروهای تغییر شکل ایجاد کرنش می کنند. نسبت تغییر طول در واحد طول است. اجباری که بر تنش منطقه ای وارد می شود. هنگامی که یک ماده تحت فشار قرار می گیرد، ضخامت ممکن است با افزایش طول کاهش یابد.
برای یک جامد همگن همسانگرد (یکنواخت)، نسبت تنش/کرنش ثابت است، مدول الاستیسیته. سه مدول الاستیسیته را توصیف می کنند: مدول یانگ (کشش طولی)، نسبت تنش به کرنش. مدول برشی یا پیچشی (سفتی)؛ و مدول حجیم یا حجمی (الاستیسیته حجمی).
الاستوگرافی فشرده (الاستوگرافی شبه استاتیک یا تصویربرداری کرنش) از تصویربرداری اولتراسوند با و بدون فشرده سازی پروب خارجی استفاده می کند. تصاویر اولتراسوند با فشرده سازی و بدون فشرده سازی ضبط می شوند. مناطق مورد علاقه مقایسه می شوند - برای تعیین تغییر شکل نسبی ارزیابی می شوند. تغییر شکل کمتری در بافتها یا ترومبهایی که سفتتر هستند دیده میشود. کرنش بافتی با اعوجاج نسبی تعیین میشود.
تصویربرداری نیروی تابشی صوتی (ARFI) از انرژی اولتراسوند تابیده شده برای حرکت بافت ها در سطح میکروسکوپی استفاده می کند. یک پرتو متمرکز اولتراسوند که از بافتهای نرم عبور میکند، در درجه اول از طریق جذب ضعیف میشود، اما برخی از فشار صوتی پرتو، حرکات بافتی را ایجاد میکند که باعث استرس تغییر شکل میشود و اثرات بیشتری بر بافتهای نرمتر دارد. این اساس نقشه برداری ARFI از سفتی بافت است. AFRI یک مقدار سختی کیفی را در امتداد محور تیر ارائه می دهد. اندازه، مکان، وسعت فضایی و مدت نیروی تابش صوتی را می توان برای ارزیابی بافت های مختلف دستکاری کرد. این تکنیک بیشتر برای ارزیابی فیبروز کبدی استفاده می شود، اما مطالعات ترومبوز وریدی از تغییرات این روش استفاده کرده است.
علاوه بر امواج فشاری که انرژی صوتی را در بافت منتشر می کنند، امواج برشی (امواج عرضی) نیز وجود دارد که در اثر نوسانات در زوایای قائم نسبت به جهت پرتو اولتراسوند ایجاد می شود. سرعت موج فشاری در بافت مربوط به مدول توده ای است، در حالی که سرعت موج برشی مربوط به مدول برشی است. از آنجایی که تغییرات در خصوصیات بافت نسبت به مدول توده ای تأثیر بیشتری بر مدول برشی دارد، تغییرات در سرعت موج برشی نشان دهنده تفاوت های ساختاری در بافت ها است. به همین دلیل، چندین روش تصویربرداری پیشرفته از امواج برشی برای توصیف بافت استفاده می کنند. مطالعات امکان سنجی با تصویربرداری الاستیسیته موج برشی (SWEI)، یا الاستوگرافی تشدید ناشی از موج برشی (SWIRE)، نشان داده است که کشش ترومبوس را می توان به صورت کمی ارزیابی کرد.
منبع : .Rosa M.S. Sigrist, Joy Liau, Ahmed El Kaffas, Maria Cristina Chammas, and Juergen K. Willmann. Ultrasound Elastography: Review of Techniques and Clinical .Applications.national library of medicine

